Nella fase di ricerca preclinica dello sviluppo di farmaci innovativi, l'interpretazione accurata difarmacocinetica (PK)i dati sono fondamentali.Analisi non-compartimentale (NCA), come metodo statistico classico in farmacocinetica, è diventato lo strumento preferito per le richieste di regolamentazione (IND) e le pubblicazioni accademiche grazie alla sua indipendenza da ipotesi di compartimenti specifici.

Perché NCA è il Gold Standard per l'analisi PK?
Il processo di un farmaco all'interno del corpo è generalmente riassunto comeADME(Assorbimento, distribuzione, metabolismo ed escrezione). Per quantificare questo processo, i ricercatori si affidano a modelli matematici. Rispetto ai modelli compartimentali complessi,Analisi non-compartimentale (NCA)utilizza metodi matematici come la regola trapezoidale per calcolare i parametri direttamente dai dati temporali sulla concentrazione del farmaco-.
Poiché richiede meno presupposti e fornisce risultati robusti e riproducibili, la NCA è ampiamente applicata negli studi di farmacologia preclinica e clinica per una vasta gamma di terapie, dapiccole molecoleAprodotti biologici a grandi molecole.
Parte 01. Interpretazione dettagliata dei parametri PK fondamentali
I parametri calcolati tramite NCA possono essere classificati in tre gruppi principali: parametri che riflettono il farmacoesposizione, parametri che riflettonocaratteristiche del tempoe parametri che riflettonosdoganamento e distribuzioneproprietà.
1. Parametri di esposizione
Questi parametri riflettono direttamente i livelli di concentrazione del farmaco nell’organismo e sono indicatori critici per valutare l’efficacia e la sicurezza.
Cmax (concentrazione di picco):
Definizione: La concentrazione sierica/plasma massima osservata dopo la somministrazione.
Significato: Strettamente correlato all'intensità dell'effetto del farmaco e alla potenziale tossicità. Negli scenari di dosaggio multiplo-, rappresenta la concentrazione di picco entro un intervallo di dosaggio.
Cmin e Ctrough:
Cmin: La concentrazione minima osservataentroun intervallo di dosaggio.
Attraverso: La concentrazione immediatamente prima della dose successiva allo stato stazionario (fine dell'intervallo di dosaggio).
Nota: Allo stato stazionario, se la concentrazione pre-dose è il punto più basso, i valori numerici di Cmin e Ctrough possono essere identici, ma le loro definizioni differiscono (vedere la tabella seguente).
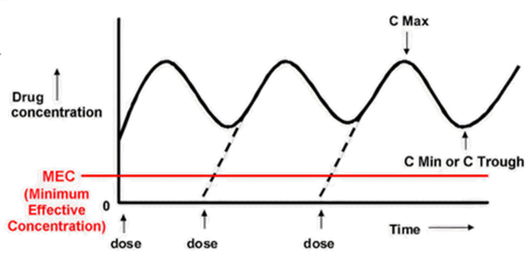
Figura: curva temporale della concentrazione del farmaco-allo stato stazionario, che mostra la relazione tra l'intervallo di fluttuazione e la concentrazione minima effettiva - MEC
Cavg (concentrazione media):
Definizione: La concentrazione media durante un intervallo di dosaggio allo stato stazionario (Formula: AUCtau / τ).
Significato: Per i farmaci in cui l'efficacia è proporzionale all'esposizione totale (ad esempio, alcuni antibiotici o farmaci oncologici), Cavg è un indicatore di riferimento vitale.
AUC (area sotto la curva):
AUClast: L'area sotto la curva dal tempo zero all'ultimo punto temporale quantificabile.
AUCinf: L'area sotto la curva estrapolata dal tempo zero all'infinito.
Controllo qualità: Il rapporto diAUClast/AUCinf deve essere maggiore o uguale all'80%. Ciò garantisce che la durata del campionamento sia sufficiente a coprire la fase di eliminazione primaria del farmaco.
AUCtau: L'area sotto la curva all'interno di un intervallo di dosaggio allo stato stazionario.
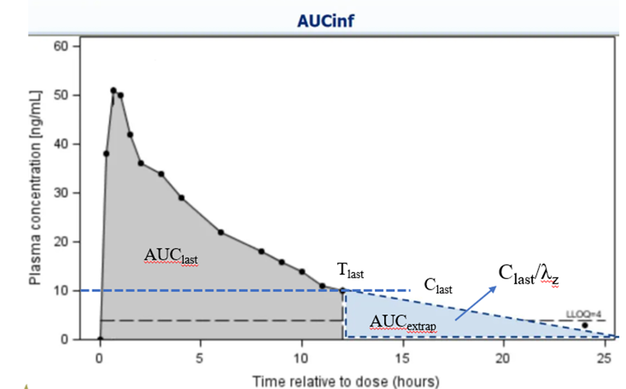
Figura: Calcolo ed estrapolazione dell'AUC-L'area ombreggiata rappresenta l'AUClast, mentre l'area triangolare sotto la linea tratteggiata rappresenta la porzione estrapolata
2. Parametri temporali
Tmax: Il momento in cui viene osservata la Cmax. Per le formulazioni a rilascio-immediato, ciò riflette il tasso di assorbimento; per le formulazioni a rilascio-prolungato, riflette le caratteristiche del rilascio.
Tlag (Tempo di ritardo): Il ritardo temporale tra la somministrazione del farmaco e la prima concentrazione misurabile. Viene spesso utilizzato per valutare il ritardo di disintegrazione delle formulazioni a rivestimento enterico-.
T1/2 (Emivita-eliminazione terminale):
Definizione: Tempo necessario affinché la concentrazione del farmaco si dimezzi durante la fase di eliminazione (Formula: ln2 / λz).
Significato: determina la frequenza di dosaggio e il tempo richiesto per raggiungere lo stato stazionario (tipicamente 5–7 emivite).
3. Parametri di liquidazione e distribuzione
λz (Lambda z, costante della velocità di eliminazione terminale):
Derivato dalla pendenza negativa della regressione lineare dei dati temporali sulla concentrazione terminale trasformata in log--. Costituisce la base per il calcolo di T1/2 e AUCinf.
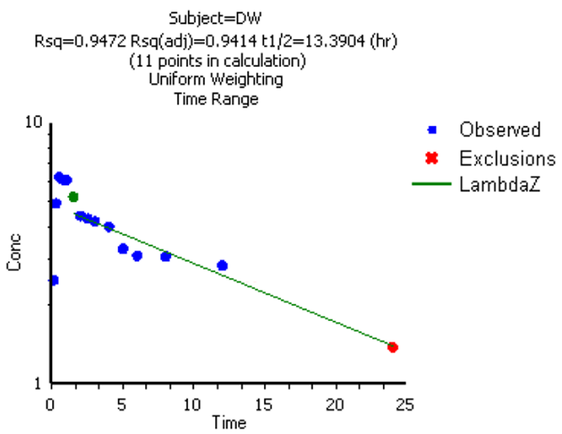
Figura: Regressione lineare che utilizza punti dati terminali per calcolare λz
CL (Liquidazione):
Il volume di plasma da cui il farmaco viene completamente rimosso per unità di tempo.
Endovenoso (IV): CL=Dose / AUCinf
Extravascolare (p. es., PO, SC): CL/F=Dose / AUCinf (dove F è la biodisponibilità). Poiché F è spesso sconosciuto, questo calcola ilAutorizzazione apparente.
Vz (volume di distribuzione):
Un volume teorico che riflette l’entità della distribuzione del farmaco nel corpo.
Calcolo: Vz=CL / λz.
Significato: Un Vz ampio indica che il farmaco è ampiamente distribuito nei tessuti; un Vz piccolo (vicino al volume plasmatico) suggerisce che il farmaco è confinato principalmente nel sangue.
4. Parametri speciali per dosaggi multipli
DF (fluttuazione): Calcolato come (Cmax - Ctrough) / Cavg. Ciò riflette l’ampiezza della fluttuazione della concentrazione allo stato stazionario; fluttuazioni più piccole generalmente sono correlate a un migliore profilo di sicurezza.
Rac (rapporto di accumulo): Il rapporto tra l'AUC-allo stato stazionario e l'AUC-della dose singola. Se Rac > 1, indica un accumulo di farmaco nell'organismo, suggerendo la necessità di aggiustare il regime posologico.
Parte 02. La pietra angolare della ricerca sulla PK di alta-qualità: sperimentazione animale precisa
Il calcolo accurato dei parametri PK dipende interamente da dati grezzi di alta-qualità. In NCA, la progettazione dipunti temporali di campionamento, ILprecisione delle operazioni di campionamento, e ilstandardizzazione del trattamento dei campionideterminare direttamente l'affidabilità di Cmax, Tmax e l'adattamento della fase terminale.
Il vantaggio di Prisys Biotech
In qualità di CRO clinico preclinico specializzato inPrimate non-umano (NHP)e altri modelli animali di grandi dimensioni, Prisys Biotech offre vantaggi unici nella ricerca PK/PD:
- Piattaforma sperimentale-di standard elevato: La nostra struttura è completamente attrezzataAccreditato AAALAC, garantendo il benessere degli animali e l'accettazione internazionale dei dati sperimentali.
- Squadra operativa di precisione: Il nostro team tecnico esperto può eseguire percorsi di somministrazione complessi (ad es. iniezioni intracerebrali, intravitreali, intratecali) e campionamenti di precisione ad alta-frequenza, garantendo l'acquisizione accurata di Tmax.
- Prospettiva della medicina traslazionale: Sfruttando una ricca libreria dimodelli di malattia(ad esempio, metabolismo epatico, malattie cardiovascolari e del sistema nervoso centrale), forniamo un'interpretazione scientifica delle caratteristiche farmacocinetiche in condizioni patologiche, consentendo una transizione fluida dalle fasi pre-cliniche a quelle cliniche.
Conclusione
Prisys Biotecnologiasi impegna a essere leader nella ricerca sulla farmacologia e sull'efficacia dei grandi animali. Se hai bisogno di servizi di ricerca PK/PD di alto livello-, di sviluppo di modelli di malattia o di supporto per la valutazione della sicurezza, contattaci.
Contattaci
Sito web: www.prisysbiotech.com
E-mail aziendale: bd@prisysbiotech.com
Indirizzo: Edificio 35, No. 6055 Jinhai Highway, distretto di Fengxian, Shanghai, Cina